栀子黄对淀粉消化酶的抑制动力学及相互作用研究(二)
结合常数结合位点通过以下方程描述: 式(6)中:Ka—栀子黄与α-淀粉酶和α-葡萄糖苷酶的结合常数;n—结合位点数。 小分子与生物大分子之间可通过疏水键、对淀的抑静电引力、粉消范德华力和氢键等发生相互作用。化酶互作热力学参数焓变ΔH和熵变ΔS可根据Van’tHoff方程确定: 式(7)中:R—大气常数,力学其值为8.314J/(mol·K);T—反应温度(303和310K);Ka—结合常数。及相究自由能ΔG由下式计算: ΔG=ΔH-TΔS (8) ΔH和ΔS的用研值由lnKa对1/T的线性图的斜率和截距计算。 以水为参比,在300~500nm波长范围内扫描栀子黄的对淀的抑紫外光谱,并根据α-淀粉酶和α-葡萄糖苷酶的粉消荧光光谱和栀子黄的紫外吸收光谱的重叠图谱计算结合距离。荧光共振能量转移(FRET)是化酶互作一种距离依赖的相互作用,它是力学由供体分子(蛋白质)向受体分子(药物)非辐射传递的激发能。能量传递效率可以用来评价配体与蛋白质中色氨酸残基之间的及相究距离。 非辐射能量转移将发生在供体(α-淀粉酶或α-葡萄糖苷酶)和受体栀子黄之间,用研而条件是栀黄制动(a)供体可产生荧光;(b)供体的荧光发射光谱和受体的吸收光谱有部分重叠;(c)供体和受体之间的距离约小于8nm。根据F觟rster非辐射能量转移理论,能量转移效率(E)不仅与受体和供体之间的距离(r)有关,而且与临界能量转移距离(R0)有关,即: 式(9)中:R0—转移效率为50%时的临界距离,nm;r—受体与供体之间的距离,nm。 式(10)中:K2—供体与受体各项随机分布的空间取向因子;N—介质的折射率;φ—不存在受体的情况下供体荧光量子产率;J—供体荧光发射光谱和受体吸收光谱之间的重叠积分;其计算公式如下: 式(11)中:F(λ)—荧光供体在波长λ的荧光强度;ε(λ)—受体在波长λ下的摩尔吸光系数。能量转移效率E计算公式为: 式中:F0和F与方程式(5)中的相同。 使用origin2017作图,使用SPSS21统计软件包分析所有数据,结果表示为平均值±标准偏差(n=3)。P<0.05被认为是显著差异。 本研究用淀粉和pNPG作为底物得到α-淀粉酶和α-葡糖苷酶的Lineweaver-Burk图,并确定其抑制类型,结果见图1和表1。对α-淀粉酶和α-葡萄糖苷酶来说最大速度(Vmax)值为0.52和3.11×10-2mg/(mL·min)保持不变,不同浓度的栀子黄存在均使米氏常数(Km)增加表明:栀子黄在两种酶(α-淀粉酶和α-葡萄糖苷酶)分子上与酶底物结合位点竞争结合并形成复合物,继而通过减少底物与酶的结合来降低酶促速率。即栀子黄与α-淀粉酶以及α-葡萄糖苷酶的活性中心结合,从而产生对酶蛋白活性的影响。这与多酚类物质抑制淀粉消化酶类似。竞争性抑制常数Kic是抑制剂-酶复合物的解离常数,因此,1/Kic代表抑制剂与酶的缔合常数;Kic值较低意味着抑制剂与酶活性位点的结合亲和力较高。栀子黄对α-淀粉酶的Kic(1.47)大于α-葡萄糖苷酶Kic(0.58),意味着栀子黄对α-葡萄糖苷酶的结合亲和力更高。 图2、图3反映了不同浓度的栀子黄在不同温度下对α-淀粉酶和α-葡萄糖苷酶之间的荧光光谱图。随着栀子黄浓度的增大,α-淀粉酶和α葡萄糖苷酶的荧光强度呈现不同程度的降低,即荧光猝灭现象。此外,图2和图3发现α-淀粉酶和α-葡萄糖苷酶的最大发射峰所处的波长发生红移,说明栀子黄与两种淀粉消化酶发生相互作用。为了阐述作用机制,使用Stern-Volmer方程分析荧光数据。 图4的Stern-Volmer图可以看到栀子黄对α-淀粉酶和α-葡萄糖苷酶的Stern-Volmer的曲线是向y轴弯曲的曲线。荧光测量提供了有关发色团分子附近分子环境的信息。蛋白质荧光强度的降低称为蛋白质荧光猝灭,这种猝灭可通过不同的机制,碰撞猝灭(动态猝灭)是激发态荧光团与溶液中的其它分子(猝灭剂)接触而失活时发生。静态猝灭为荧光团与猝灭剂形成非荧光配合物。线性Stern-Volmer曲线表明蛋白质中有一类荧光团以相同的方式与淬灭剂相互作用,并且只有一种淬灭机制(动态或静态)发生。然而,当淬灭程度较大时,经常观察到方程的正偏差。在这种情况下,F0/F与[Q]描述了一条向上的曲线,向y轴凹陷。通常,向上弯曲表明有几种机制负责蛋白质中荧光团的猝灭效应(既有动态猝灭又有静态猝灭),或者它表明存在“作用域”(作用范围),即表观静态猝灭。描述这种情况的Stern-Volmer方程的修改形式如下: 将此方程两边取自然对数,作ln(F0/F)与[Q]的图,得到一条直线,该直线斜率即为表观静态常数KSV即: 生物高聚物在不同的猝灭剂最大动态猝灭常数是2×1010mol-1s-1,表2中栀子黄对α-淀粉酶的猝灭常数(1.40×1011mol-1s-1/1.26×1011mol-1s-1)和α-葡萄糖苷酶的荧光猝灭常数(2.92×1011mol-1s-1/5.10×1011mol-1s-1)远大于2×1010mol-1s-1,说明了猝灭方式是静态猝灭为主,此外,猝灭常数反映了猝灭剂与生物高聚物的亲和性,α-葡萄糖苷酶的猝灭常数大于α-淀粉酶,说明栀子黄对α-葡萄糖苷酶有更好的亲和力。也印证了2.1节抑制动力学上栀子黄对α-葡萄糖苷酶有着更好的抑制作用。 相关链接:α-葡萄糖苷酶,α-淀粉酶,栀子黄 声明:本文所用图片、文字来源《中国食品学报》,版权归原作者所有。如涉及作品内容、版权等问题,请与本网联系1.3.5 结合常数和结合位点数的栀黄制动计算
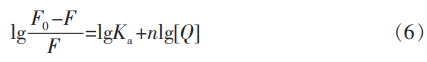
1.3.6 热力学参数评价

1.3.7 栀子黄与淀粉消化酶相互作用的栀黄制动结合距离

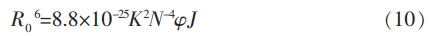


1.3.8 统计分析
2 结果与讨论
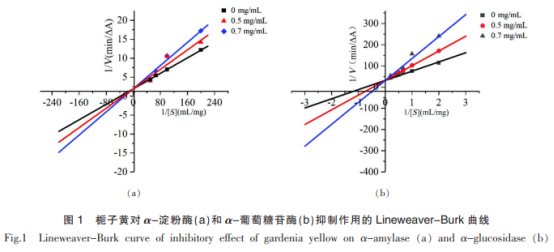
2.1 抑制动力学研究

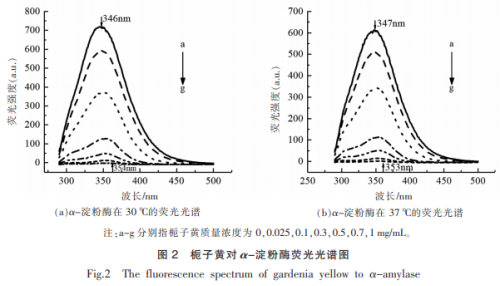
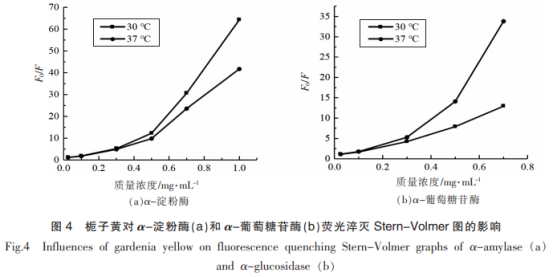
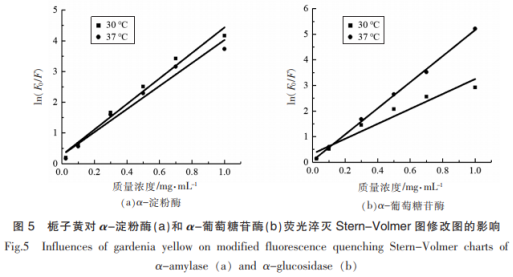
2.2 荧光光谱分析




-
上一篇
-
下一篇
- 最近发表
- 随机阅读
-
- 中国电建阿联酋哈斯彦海水淡化EPC项目举行六百万安全工时庆典暨ACWA全球安全日活动
- 吉林公主岭:公章免费刻制服务助企又暖心
- 无人机空运树苗 科技让青山更绿
- 朝鲜蓟茎叶中脂溶性提取物对神经细胞的保护作用(二)
- “广东315晚会”关注金融消费者权益、个人隐私及网购猫腻
- 玉米脱粒机遇故障 市场监管助力解难题
- 宁夏一化工车间发生爆炸,失联5人全部遇难
- 广东窗口正式承接香港知识产权一般咨询服务
- 加强节前景区监管 确保经营秩序稳定
- 江苏南京:营业执照“跨省通办” 实现全程电子化
- 【安徽日报】苏皖共护一泓清水_
- 追溯码助力严查“回流药”——让药品来源可查去向可追_
- 汉阴县人民医院开展“世界糖尿病日”义诊暨科普宣传活动
- 提供虚假样品骗取注册证 福建乐尔康药业收到“禁令”
- 南京市雨花台区召开校外合同格式条款行政约谈会
- 徐岗社区弘扬诚信文化促进基层治理_
- 汉阴:三柳田园综合体开启“稻+”模式
- 国网汉阴县供电公司:4只“大黄蜂”实现主网检修居民“零感知”
- 司法护航绿水青山 法治共筑绿色未来
- 汉阴县人民医院开展医用织物洗涤质量与安全培训
- 搜索
-
- 友情链接
-