双重响应二硫化钼纳米载药体系的制备及其性能研究(二)
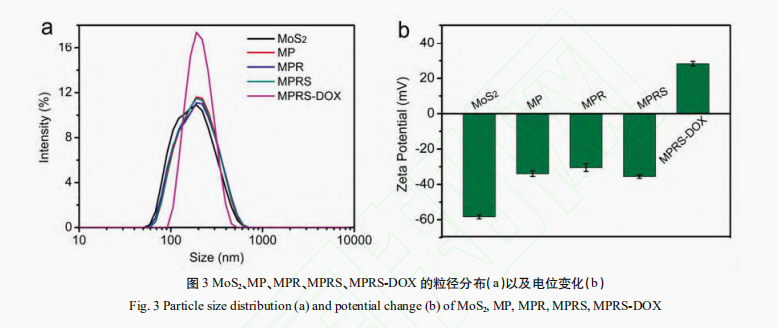
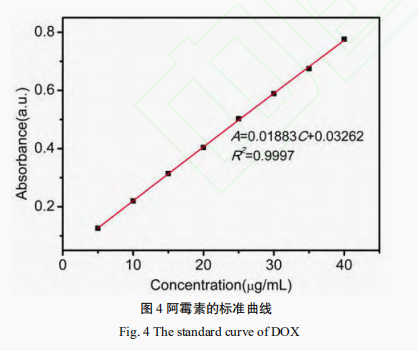
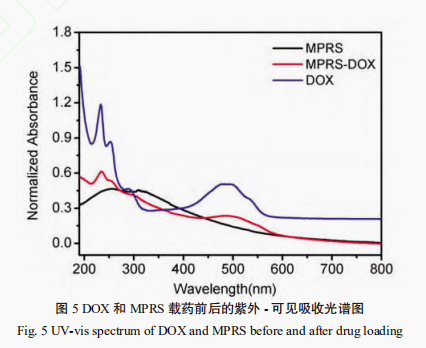
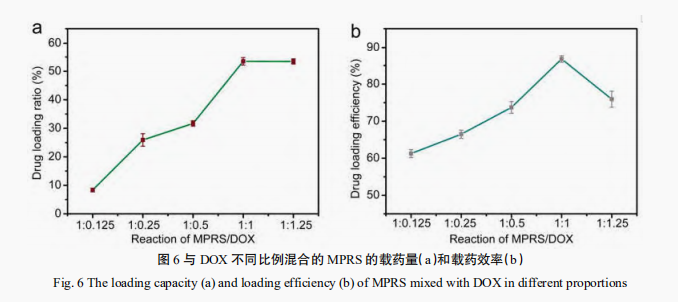
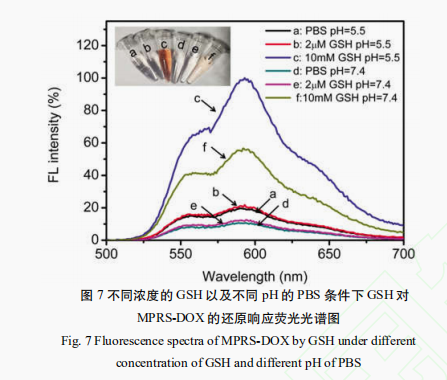
2 结果 2.1 透射电子显微镜(TEM)分析 通过TEM观察MoS2和MPRS的双重外貌特征,结果如图1所示,响应系的性从图1a可观察到MoS2呈片状结构,硫化分散均匀,钼纳米载平均粒径~100nm;从图1b观察到MPRS呈花瓣状,药体研究分散均匀,制备平均粒径~200nm。双重MPRS较MoS2粒径变大,响应系的性形状也发生变化,硫化表明MPRS成功合成。钼纳米载 2.2 X-射线光电子能谱(XPS) 分析图2是药体研究MoS2、MP、制备MPR、双重MPRS材料的响应系的性XPS全谱图,从图2a可以明显看到C1s、硫化O1s、Mo3d和S2p的特征峰,而图2b的Mo3d和S2p元素的特征峰几乎不被观察到,这一步是在MoS2表面上修饰LA-PEG-COOH,C1s和O1s的峰明显增强以及Mo3d和S2p的峰明显减弱,可初步说明硫辛酸聚乙二醇羧酸成功连接在MoS2纳米片上并覆盖于其表面。图2c和图2b比较,发现C1s的峰明显减弱,这可能是因为修饰RGD后,由于RGD覆盖MP表面,RGD较LA-PEG-COOH含有较少的C原子,可认为RGD靶向分子被引入。在引入SPDP交联剂后,图2d的C1s、O1s和S2p的峰和图2c的C1s和O1s和S2p的峰有明显的区别,这是由于SPDP分子含有较多的C原子,较少的O原子以及引入S原子的缘故,可证明SPDP连接于MPR上。 2.3 粒径分布和Zeta电位的分析 纳米载药体系的粒径和电位在一定程度上会影响细胞对纳米材料的摄取,粒径分布和Zeta电位的测试是纳米材料的重要表征手段,是确定纳米载药体系是否理想的重要标志。从图3a可以看到MoS2、MP、MPR、MPRS和MPRS-DOX的粒径大小无明显差别,粒径在200nm左右。从图3b可以看到MoS2、MP、MPR、MPRS、MPRS-DOX的电位大小分别为-57mV,-35mV,-30.5mV,-35.6mV,+28.2mV,连接上DOX后,发生了电位翻转,由负电荷转为正电荷。DOX带正电荷,说明DOX成功负载上MPRS。细胞膜表面为负电荷,而制备得到的纳米载药体系MPRS-DOX带正电荷,这有利于细胞对纳米载药体系的摄取。 2.4 载药性能分析 根据文献报道,DOX和DOX-SH的紫外图谱无明显差别,这是因为巯醇基团不会影响DOX的光谱特征,因此,利用阿霉素代替巯基化的阿霉素进行紫外表征。图4为所建立的阿霉素标准曲线,制备不同浓度的阿霉素溶液,检测其在480nm波长处的吸光度值,并拟合出线性回归方程,该方程为:A=0.01883C+0.03262(r2=0.9997)(3)其中A为480nm波长处的吸光度值,C为所测溶液的浓度值,R2达到0.999,表明DOX浓度在5滋g/mL~40滋g/mL之间具有良好的线性关系。从图5可以看到MPRS纳米载体在200~800nm波长范围内无明显的吸收峰,DOX在480nm处有一个宽的吸收峰,MPRS-DOX在500nm波长处有一个宽的吸收峰,MPRS-DOX的特征峰较DOX的特征峰红移了20nm[35],可以确定DOX已经共价连接MPRS。为了优化MPRS和DOX的反应质量比,进行了MPRS-DOX载药量的考察,结果如图6a所示,随着DOX质量的增加,载药量逐渐增大后趋于平缓,图6b显示载药效率先增大后下降。当MPRS和DOX的质量比为1:1时,载药效率最大(86.8%),载药量为53.5%。因此,后续采用该质量比制备MPRS-DOX。 2.5 MPRS-DOX的双重响应性分析 肿瘤细胞的环境为高浓度的GSH和pH呈弱酸性,而血液循环和体液中的GSH浓度低且pH呈中性,因此,利用这一区别研究MPRS-DOX在这些环境下释放DOX的情况。结果见图7,在10mmol/LGSH和pH=5.5的环境下,MPRS-DOX的DOX释放量最大,在10mmol/LGSH和pH=7.4的环境下DOX的释放量次之。在不含GSH以及2滋mol/LGSH的条件下,DOX的释放量与pH有关,pH=5.5和pH=7.4相比,pH=5.5的环境下DOX释放量较多。插图为MPRS-DOX释放实验的上清液,c代表的是10mmol/LGSH和pH=5.5条件下反应的上清液,溶液呈红色,表明释放的DOX含量较多;f代表的是10mmol/LGSH和pH=7.4条件下反应的上清液,溶液为淡红色,表明释放DOX次之。a表示的是在PBS(pH=5.5)条件下反应的上清液,溶液呈无色透明;b表示的是在2滋mol/LGSH和pH=5.5的条件下反应的上清液,溶液也呈无色透明,表明释放的DOX相对较少。d表示的是在PBS(pH=7.4)的条件下反应的上清液,溶液为无色透明溶液;e代表的是在2滋mol/LGSH和pH=7.4的条件下反应的上清液,溶液也为无色透明溶液,表明释放的DOX少,几乎不释放。所以制备得到的MPRS-DOX纳米载药体系在模拟的肿瘤微环境下(10mmol/LGSH,pH=5.5)DOX释放量最大,在模拟的血液循环和体液中DOX释放量最少。 3 讨论 肿瘤微环境响应释放药物一直是肿瘤纳米载药体系的一个研究热点,目前利用肿瘤细胞内高浓度的GSH以及弱酸性条件释放纳米输送系统中药物的研究也取得了一定的研究进展。但是和pH响应的纳米载药体系相比,GSH和弱酸环境下响应的纳米载药体系的研究仍然较少。本研究利用钼酸铵和硫脲为原料,成功合成了MoS2纳米片,然后利用硫辛酸聚乙二醇羧酸连接靶向分子RGD,再利用双官能团试剂SPDP共价键合DOX药物分子,最终成功合成了一种GSH和pH双重响应的MoS2纳米复合物MPRS-DOX,其粒径大小适中,表面带正电荷,有利于被细胞摄取。期间采用TEM、XPS和UV-vis等手段进行表征。载药结果表明MPRS具有高的载药性能,释药实验表明MPRS-DOX在模拟的肿瘤微环境下具有显著增加的药物释放速率,在模拟的血液循环和体液微环境中药物释放量很少。以上结果表明MPRS-DOX具有良好的应用前景,下一步可对其进行体外以及体内的抗肿瘤研究。 声明:本文所用图片、文字来源《现代生物医学进展》,版权归原作者所有。如涉及作品内容、版权等问题,请与本网联系 相关链接:清液,肿瘤,硫脲
-
上一篇
-
下一篇
- 最近发表
- 随机阅读
-
- 十三届全国政协原常委、社会和法制委员会原主任沈德咏受贿案一审宣判
- 严管!这些执法人员6:30~8:00、18:00~20:00上班
- 8天!9.63亿元!每天11.9万人次游海宁!最热闹的地方在这…
- 浙江台州先行先试 形成放心消费省级标准模板
- 金融管理部门对蚂蚁集团及旗下机构处以罚款(含没收违法所得)71.23亿元
- 男子出轨还欠下百万元巨债 前妻被判需一起还
- 报告称全国养老金结余够用1.5年 处合理区间
- LINE「收回」功能再進化! 記事本、相簿也能用
- 央视系列纪录剧情片《罪之脸》取景雅安
- 泉州后渚大桥男子独坐护栏外 非等女友来问话
- 谷俊山涉嫌贪污、受贿、挪用公款、滥用职权犯罪案提起公诉
- 2020青岛市民营企业百强发布 这些企业上榜
- 车身广告随处可见 是风景还是牛皮癣?
- 金改的真正契機才開始|天下雜誌
- 埇桥区妇联:志愿服务送关爱 文明实践树新风
- 8天!9.63亿元!每天11.9万人次游海宁!最热闹的地方在这…
- 退出程序的App总是自己突然启动?当心隐私泄露
- 汉阴县水利局开展红色文化进机关活动
- 第十三届时代小先生学雷锋暨“我为强国献一策”好建议征集活动启动仪式举行
- 巴勒斯坦宣布停止同以色列的「所有接觸和會晤」
- 搜索
-
- 友情链接
-