HPLC法同时测定引阳索中五味子醇甲、五味子乙素的含量
目的法同:建立HPLC法同时测定引阳索中五味子醇甲、五味子乙素的时测素含量。方法:采用AgilentExtendC18(250mm×4.6mm,定引5μm)色谱柱;以甲醇-乙腈-0.1%磷酸溶液为流动相,阳索流速为1.1mL·min-1;梯度洗脱;进样量为10μL;检测波长为250nm;柱温为32℃。中味结果:五味子醇甲、醇甲五味子乙素的味乙线性范围分别为7.013~175.3mg·L-1(r=0.9998,n=7)和7.040-176.0mg·L-1(r=0.9998,含量n=7);提取回收率:五味子醇甲96.05%(RSD=0.7%,法同n=6),时测素五味子乙素96.48%(RSD=0.9%,定引n=6)。阳索结论:本法操作专属性强、中味快速、醇甲简便、味乙结果准确,可用于引阳索的质量控制。 1仪器 Waters2695高效液相色谱仪(包括工作站、自动进样、柱温箱、2998型二极管阵列检测器美国Waters公司),XPE205电子天平(METTLERTOLEDO公司),超声波清洗机(HT300功率:40KHZ济宁恒通超声电子设备),超纯水机(Milli-QAdvantageA10默克密理博公司)。 2材料 五味子醇甲对照品(批号110857-201010含量99.4%)、五味子甲素对照品(批号110764-201010含量99.6%)、五味子乙素对照品(批号110765-200710)均购自中国药品生物制品检定所,引阳索药品3批(批号:20170704,20180604,20191103,市售),淫羊藿(批号:1910001,安国市聚药堂药业有限公司),超纯水(自制),其他试剂(色谱纯,市售)。 3方法和结果 3.1色谱条件与系统适用性试验 色谱柱:AgilentExtendC18柱(250mm×4.6mm,5μm);流动相:甲醇(A)-乙腈(B)-0.1%磷酸溶液(C),梯度洗脱:0~24min为35%~55%A,30%~30%B;24~27min为55%~35%A,30%~30%B;27~30min为35%~35%A,30%~30%B;检测波长:250nm;流速:1.1mL·min-1;进样量:10μL;柱温:32℃。五味子醇甲、五味子乙素与相邻色谱峰的分离度均大于1.5,理论板数均不低于5000。 3.2溶液的制备 3.2.1对照储备液 取P2O5干燥13h的五味子醇甲、五味子甲素、五味子乙素对照品,分别精密称取14.11mg、16.62mg、14.08mg置20mL量瓶中,加甲醇适量,超声使溶解,用甲醇稀释至刻度,作为对照品储备液(五味子醇甲701.3mg·L-1,五味子甲素827.7mg·L-1,五味子乙素704.0mg·L-1)。分别精密量取1mL,置同一10mL量瓶中,用甲醇稀释至刻度,得混合对照品溶液。 3.2.2供试品溶液 取供试品5袋,精密称重,研细,精密称取5g(相当于1袋),置100mL具塞锥形瓶中,加体积分数75%甲醇溶液50mL,密塞,称重,超声提取30min;放置至室温,称定重量,用上述甲醇溶液补足减失重量,用0.45μm微孔滤膜过滤,备用。 3.2.3阴性对照溶液 3.3线性关系考察 依次精密量取五味子醇甲、五味子乙素对照品储备液各0.1、0.2、0.5、1.0、1.5、2.0、2.5mL,分别置10mL量瓶中,用甲醇稀释至刻度,摇匀,得不同浓度系列混合对照溶液。按“3.1”条色谱条件,进样10μL,以峰面积(Y)对质量浓度X(mg·L-1)进行回归分析,得:五味子醇甲回归方程Y=2.062×104X-7.829×104(r=0.9998,n=7),在7.013~175.3mg·L-1内,五味子醇甲线性良好;五味子乙素回归方程Y=1.543×104X-6.039×104(r=0.9998,n=7),在7.040~176.0mg·L-1内,五味子乙素线性良好。 3.4精密度试验 取五味子醇甲、五味子乙素混合对照品储备液,用0.45μm微孔滤膜滤过,按“3.1”条色谱条件,连续进样5次,每次10μL,测得五味子醇甲峰面积分别为1386130、1413230、1416601、1409903、1398858,RSD为0.9%(n=5);五味子乙素峰面积分别为1039735、1068231、1064348、1059376、1053065,RSD为1.1%(n=5),结果表明仪器有良好的精密度。 3.5稳定性试验 取引阳索颗粒适量,按“3.2.2”条方法制备供试溶液,依次在0、2、6、10、18、24、48h,重复进样,每次10μL,测得五味子醇甲峰面积分别为1439032、1428035、1419366、1418367、1421035、1416534、1403982,RSD为0.8%(n=7);五味子乙素峰面积分别为505762、504927、506354、498756、492769、503262、491965,RSD为1.2%(n=7),结果表明样品在48h内稳定。 3.6重复性试验 分别精密称取同一批引阳索(批号20180604)5份,按“3.2.2”条方法制备供试溶液,测量五味子醇甲含量分别为3.63、3.68、3.67、3.69、3.64mg/袋,RSD为0.7%(n=5),五味子乙素含量分别为1.82、1.81、1.79、1.83、1.84mg/袋,RSD为1.0%(n=5),结果表明方法重复性良好。 3.7回收率试验 分别精密称取已知含量的引阳索(批号20180604)约2.5g,6份,分别置100mL锥形瓶中,分别精密加入对照溶液:五味子醇甲对照溶液(0.9165mg·mL-1)、五味子乙素(0.9118mg·mL-1)、各2.0、1.0mL,按“3.2.2”条方法制备供试溶液,进样10μL,结果测得五味子醇甲、五味子乙素平均回收率分别为96.05%(RSD=0.7%,n=6)、96.48%(RSD=0.9%,n=6),结果见表1。 4.1测定波长的选择 宣东平等报道了五味子醇甲和五味子乙素同时检测的波长为254nm,《中国药典》2015版五味子含量测定项下测定五味子醇甲的波长为250nm,综合考虑被测物质最大吸收波长、吸收强度,最终选定250nm作为检测波长。 4.2流动相的选择 流动相比较了甲醇-0.1%磷酸溶液(35:65)、乙腈-0.1%磷酸溶液(30:70),发现被测成分可以达到基线分离,但五味子乙素保留时间超过60min,与杨立志等研究结果相同,最终选择甲醇-乙腈-0.1%磷酸溶液三元系统为流动相,梯度洗脱,流动相通过引入乙腈缩短被测物质保留时间,线性调整甲醇和0.1%磷酸溶液比例使3种木脂素与其他物质有效分离,结果样品中五味子醇甲、五味子甲素和五味子乙素分离效果好,无杂质干扰,且出峰快,保留时间分别为五味子醇甲5.18min、五味子甲素16.88min、五味子乙素20.35min。 4.3含量测定指标选择 任伟光等报道了五味子醇甲、甲素、乙素是五味子中重要木脂素类化合物,有保护肝脏、中枢抑制、降糖、抗炎等药理作用。马莹慧等报道了五味子醇甲、醇乙、酯甲、甲素、乙素为指标的含量分析方法,李宝等报道了五味子浸膏中五味子醇甲、甲素、乙素的含量测定方法,本研究发现引阳索样品色谱图中五味子甲素色谱峰峰面积较小,因此本文仅选择了五味子醇甲和五味子乙素2个指标进行含量测定。五味子甲素色谱峰可作为特征峰之一,用于引阳索中五味子浸膏的定性鉴别。 声明:本文所用图片、文字来源《黑龙江医药》,版权归原作者所有。如涉及作品内容、版权等问题,请与本网联系删除 相关链接:五味子乙素,色谱,乙腈
引阳索收载于《中华人民共和国卫生部药品标准》中药成方制剂第三册,由淫羊藿浸膏与五味子浸膏按2∶1混合制成颗粒剂,具有补肾壮阳,生津功能,用于阳痿早泄,腰膝酸软,津亏自汗,头晕目眩等症。现行标准中缺少对处方中五味子浸膏质量控制的方法,谭文明和孟淑智先后报道了引阳索中五味子浸膏指标成分五味子甲素和五味子醇甲的TLC鉴别方法,目前尚未有引阳索中五味子浸膏指标成分五味子醇甲和五味子乙素含量测定的报道,本文建立了同时测定引阳索中五味子醇甲和五味子乙素的含量方法,本研究专属性强,可用于引阳索中五味子浸膏的质量控制。
按引阳索处方,不加五味子浸膏,按“3.2.2”条方法制备阴性对照溶液。按“3.1”条色谱条件进样,记录色谱图见图1。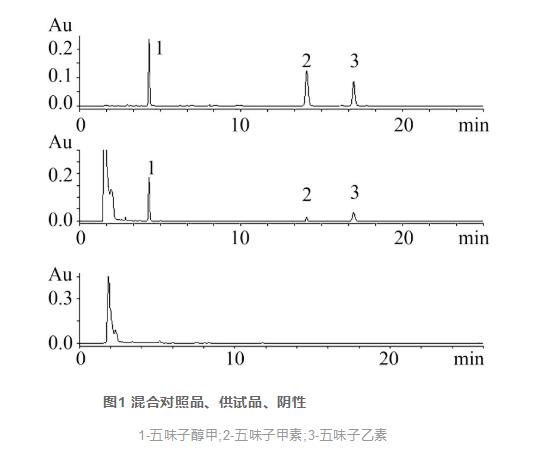

3.8样品含量测定
取引阳索10袋,按“3.2.2”条方法制备供试溶液,平行3份。按“3.2.1”条方法制备对照品溶液,按“3.1”条色谱条件,进样10μL,用外标法测定3批引阳索样品中五味子醇甲和五味子乙素的含量,结果见表2。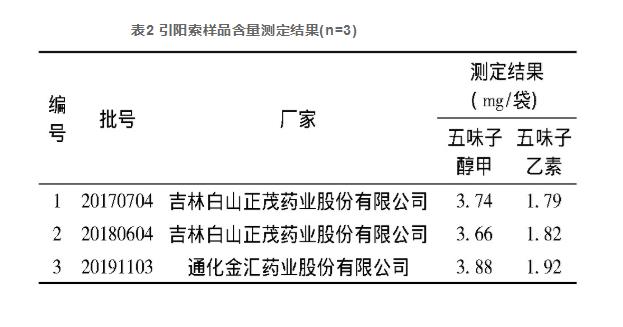
4讨论
- 最近发表
- 随机阅读
-
- 因地制宜错位发展 打造县域经济新亮点
- 新宝股份:签署谅解备忘录解决摩飞品牌国内商标使用权授权经营问题
- 网曝女童当着母亲面遭男子猥亵
- 成都本轮疫情毒株在国内无同源序列
- 北京海淀通报2起违规开展线下学科培训行为
- 基建掀起“赶工潮”稳投资展现“夏日温度”
- 女子逆行被拦停后扬言找“队长”
- 广西新增本土无症状感染者165例
- 各地市场监管部门严查野生动物销售链条
- 男子偷前同事手机进工作群骂领导
- 为儿子学费 工人高温工作9小时去世
- 船只在阳江海域走锚沉没 27人失联
- 一种燃料热沉标准物质候选物的纯度定值及不确定度分析(二)
- 华谊申请冻结密春雷公司8800万股权
- 中信信托57亿疑似无法兑付
- 女顾客掀火锅叫嚣让你从汉中消失
- 北京东城:快检元宵汤圆 保障食品安全
- 超20城发购房补贴 有人已到账10万元
- 汇川技术:已有工控整套解决方案与压铸机龙头客户产品进行匹配
- 女子发烧裹被捂汗患热射病送ICU
- 搜索
-
- 友情链接
-